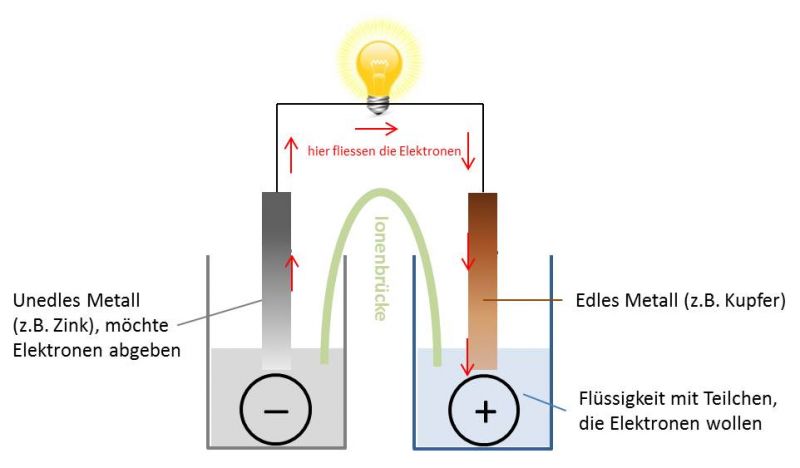
Das Prinzip der Batterie
Batterien und Akkus funktionieren nach dem Prinzip der sogenannten „Galvanischen Zelle“. Dabei sausen kleine elektrisch geladene Teilchen in einem Kreislauf umher und erzeugen Strom. Dadurch beginnt deine Taschenlampe zu leuchten oder dein iPod spielt deine Lieblingsmusik. Wie im Bild unten dargestellt, findet man in einer „Galvanischen Zelle“ zwei miteinander verbundene Gefässe mit verschiedenen Flüssigkeiten und Metallen.