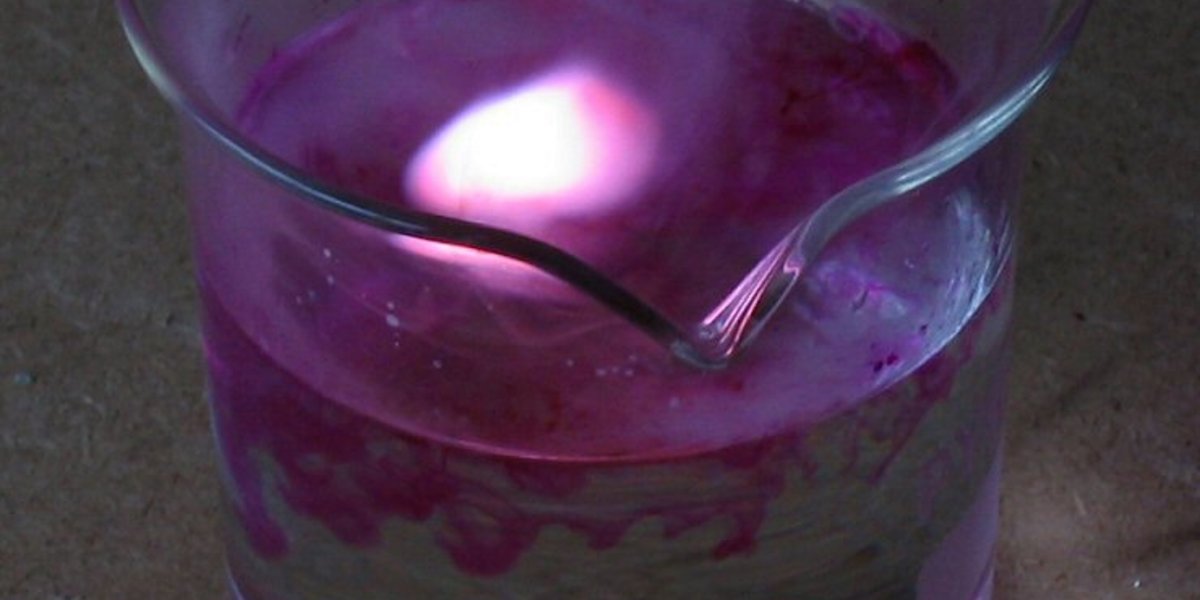
Kalium steht in der Gruppe der Alkalimetalle unter dem Natrium; sein Atomradius ist also etwas grösser und das äusserste Elektron, das Valenzelektron, ein bisschen weiter vom Kern entfernt. Dadurch erklärt sich, dass dieses Elektron noch leichter abgegeben wird und Reaktionen noch heftiger erfolgen als beim Natrium: Elementares Kalium entzündet sich beim Kontakt mit Wasser sofort, was leicht zu einer Explosion führt.
Elementares Kalium mit einer Kruste aus oxidiertem Material, die auf Druck explosiv reagieren kann. Bild: BXXXD/Wikimedia Commons, CC-Lizenz
Kleine Mengen von metallischem Kalium werden wie Lithium und Natrium in wasserfreien Flüssigkeiten wie Paraffinöl aufbewahrt; im Gegensatz zu den anderen beiden Metallen kann sich Kalium dabei aber nach einiger Zeit dennoch mit einer Kruste aus oxidiertem Material überziehen. Und dann ist Vorsicht geboten: Diese Kruste ist so empfindlich, dass sie bereits bei leichtem Druck explodieren kann!
Kaliumverbindungen: Seit langem bekannt als Dünger und Backtriebmittel
Der Name Kalium stammt vom arabischen al-qalya, was Asche bedeutet. Noch vor 200 Jahren wurde nämlich aus Holzasche durch Auswaschen und anschliessendes Eindampfen des Wassers Kaliumcarbonat (K2CO3) gewonnen. Kaliumcarbonat, auch unter dem Namen Pottasche bekannt, war und ist ein Stoff mit vielseitigen Anwendungen – sei es zum Backen von Lebkuchen, zum Sieden von Seife oder als Düngemittel. Die Tatsache, dass Kalium ein Bestandteil von Pottasche ist, spiegelt sich auch in der englischen und französischen Bezeichnung dieses Elements: Dort heisst es nämlich „potassium“.
Lebkuchen enthalten traditionell Kaliumcarbonat anstelle von Backpulver als Backtriebmittel. Bild: CanStockPhoto
Als Düngerbestandteil hat Kalium immer noch grosse Bedeutung. Im Boden ist es zwar eigentlich reichlich vorhanden, aber überwiegend in Silikat-Mineralien gebunden (beispielsweise Glimmer oder Feldspat). In dieser Form kann es von Pflanzen schwer aufgenommen werden, weshalb man dem Dünger wasserlösliche Kaliumsalze beigibt.
Kalium im menschlichen Körper
Kaliumionen sind die wichtigsten positiv geladenen Ionen in unseren Zellen; nur ein kleiner Teil der Kaliumionen befindet sich in den Körperflüssigkeiten. Ihre Konzentration innerhalb und ausserhalb der Zellen beeinflusst zahlreiche wichtige Vorgänge im Körper, zum Beispiel die Kontraktion von Muskeln und die Weiterleitung von Nervenimpulsen. Eine Flüssigkeit mit hohem Kaliumgehalt wird in der Chirurgie verwendet, um bei einer Operation am offenen Herzen einen Herzstillstand auszulösen. Der Blutkreislauf wird in dieser Zeit durch eine künstliche Pumpe aufrechterhalten. Nach Beendigung der Operation werden die Kaliumionen langsam durch Natrium ersetzt, bis das Blut wieder die gewöhnliche Konzentration an Kalium und Natrium enthält und der Herzmuskel wieder zu arbeiten beginnt.